В качестве основного лечения также используются агонисты дофаминовых рецепторов (бромокриптин, перголид , прамипексол , ропинирол , каберголин , апоморфин, лизурид ). Препараты данной группы являются специфическими центральными агонистами дофаминовых рецепторов. Имитируя действие дофамина, они вызывают те же фармакологические эффекты, что и леводопа .
По сравнению с леводопой они реже вызывают дискинезии и другие двигательные расстройства, но чаще оказывают иные побочные эффекты: отёки, сонливость, запоры, головокружение, галлюцинации, тошноту .
Ингибиторы моноаминоксидазы типа б (мао-б) и катехол-о-метилтрансферазы (комт)
Данная группа препаратов избирательно подавляет активность ферментов, которые расщепляют дофамин: МАО-Б и КОМТ. Селегилин (ингибитор МАО-Б), энтакапон и толкапон (ингибиторы КОМТ) замедляют неуклонное прогрессирование болезни Паркинсона. Фармакологические эффекты аналогичны леводопе, хотя их выраженность значительно меньше. Они позволяют усилить эффекты леводопы, не повышая и даже снижая её суммарную дозу .
Непрямые дофаминомиметики (амантадин, глудантан) повышают чувствительность рецепторов к соответствующему медиатору. Данные препараты усиливают выделение дофамина из пресинаптических окончаний и тормозят его обратный нейрональный захват. Лекарственные средства данной группы вызывают те же фармакологические эффекты, что и леводопа, то есть они преимущественно подавляют гипокинезию и мышечную ригидность, значительно меньше влияя на тремор .
Центральные холиноблокаторы
Тригексифенидил - основной препарат группы центральных холиноблокаторов, применяемых для лечения болезни Паркинсона
Для лечения паркинсонизма применяют антихолинергические средства. Знаменитый французский врач Жан Шарко ещё в 1874 году использовалбелладонну для уменьшения наблюдаемой при заболевании усиленной саливации. Им также было отмечено уменьшение тремора при её приёме. В дальнейшем для лечения стали использовать не только препараты белладонны, но и другие холиноблокаторы - атропин и скополамин. После появления синтетических холинолинолитиков стали применяться тригексифенидил (циклодол), трипериден, бипериден , тропацин, этпенал, дидепил и динезин .
Применение холиноблокаторов патогенетически обосновано. Поражения чёрной субстанции и других нервных образований приводит к существенным сдвигам в холин- и дофаминергических процессах, а именно повышению холинергической активности и снижению дофаминергической. Таким образом, центральные холиноблокаторы «выравнивают» нейромедиаторные взаимодействия .
Применяемые ранее препараты белладонны действуют преимущественно на периферические ацетилхолиновые рецепторы и меньше - на холинорецепторы мозга. В связи с этим терапевтическое действие данных препаратов относительно невелико. Вместе с этим они вызывают ряд побочных явлений: сухость во рту, нарушение аккомодации, задержку мочи, общую слабость, головокружение и др.
Современные синтетические противопаркинсонические центральные холиноблокаторы характеризуются более избирательным действием. Они широко применяются при лечении экстрапирамидных заболеваний, а также неврологических осложнений, вызываемых нейролептиками .
Отличительным свойством центральных холиноблокаторов является то, что они в большей степени воздействуют на тремор; в меньшей мере влияют на ригидность и брадикинезию. В связи с периферическим действием уменьшается слюнотечение, в меньшей степени потоотделение и сальность кожи .
В настоящее время частая причина обращения к врачам - это проблемы в работе ЖКТ. Практически для каждой из них характерно нарушение моторной функции. Однако они могут проявляться как симптомы какого-либо заболевания, не связанного с пищеварительной системой. В любом случае никак не обойтись без лекарств группы прокинетики. Список препаратов этой группы не имеет ограничительных рамок. Поэтому каждый врач подбирает препарат их в зависимости от течения заболевания. Далее рассмотрим подробнее, что такое прокинетики, список препаратов нового поколения,чаще всего используемых для лечения.
Прокинетики: общая характеристика
Лекарственные препараты, которые изменяют моторную активность кишечного тракта, ускоряют процесс транзита пищи и опорожнения, как раз и относятся к этой группе.
Как говорилось выше, единого списка этих препаратов в гастроэнтерологической литературе не существует. Каждый врач включает сюда свой список лекарств. К ним можно отнести и медикаменты других групп, таких как: противорвотные, противодиарейные, а также некоторые антибиотики группы макролиды, гормональные пептиды. Для начала выясним, в чем заключается фармакологическое действие этой группы лекарственных средств.
Действие прокинетиков
Прежде всего они активизируют моторику пищеварительного тракта, а также обладают противорвотным эффектом. Такие препараты ускоряют опустошение желудка и кишечника, улучшают мышечный тонус ЖКТ, угнетают пилорический и эзофагеальный рефлюкс. Прокинетики назначают в качестве монотерапии или в комбинации с другими лекарствами. Их можно разделить на несколько видов по принципу действия.
Виды прокинетиков
Принцип действия на разные отделы желудочно-кишечного тракта отличается у таких препаратов, как прокинетики. Список препаратов следует разделить на такие виды:
1. Блокаторы дофаминовых рецепторов:
- Селективные 1-го и 2-го поколения.
- Неселективные.
2. Антагонисты 5-НТ3-рецепторов.
3. Агонисты 5-НТ3-рецепторов.
А теперь поподробнее об этих группах.
Блокаторы дофаминовых рецепторов
Препараты этой группы делятся на селективные и неселективные. Их действие заключается в том, что они стимулируют моторную и обладают противорвотными свойствами. Какие это прокинетики? Список лекарств следующий:
- «Метоклопрамид».
- «Бромоприд».
- «Домперидон».
- «Диметпрамид».
Основное действующее вещество - метоклопрамид, его используют достаточно давно. Действие заключается в следующем:
- Повышение активности нижнего пищеводного сфинктера.
- Ускорение опустошения желудка.
- Возрастание скорости продвижения пищи по тонкому и толстому кишечнику.
Однако препараты неселективные могут инициировать серьезные побочные явления.
Есть широко известные первого поколения прокинетики. Список препаратов:
- «Церукал».

- «Реглан».
- «Перинорм».
- «Церуглан».
Один из недостатков заключается в способности вызывать признаки и симптомы паркинсонизма у взрослых и у детей, нарушение менструального цикла у женщин.
К селективным препаратам второго поколения относятся лекарства с активным действующим веществом домперидон. Эти лекарства не вызывают сильных побочных реакций, но могут проявиться другие:
- Сонливость.
- Слабость.
- Тревожность.
- Головная боль.
Именно по этой причине препараты с активным веществом домперидон - лучшие прокинетики. Список препаратов:

- «Мотилиум».
- «Домидон».
- «Мотинорм».
- «Моторикс».
- «Гастропом».
Прокинетики нового поколения
К селективным прокинетикам второго поколения относят препараты с активным веществом итоприд гидрохлорида. Такие средства завоевали признание благодаря отличному лечебному эффекту и отсутствию побочных явлений даже при длительном употреблении. Наиболее часто врачи назначают:
- «Итомед».
- «Ганатом».
- «Итоприд».
Это можно объяснить положительными свойствами итоприда гидрохлорида:
- Улучшение моторной и эвакуаторной функции желудка.
- Повышение активности желчного пузыря.
- Повышение динамичности и тонуса мышц толстого и тонкого кишечника.
- Содействие устранению
Кишечные прокинетики
Сюда можно отнести прокинетики - агонисты 5-НТ3-рецепторов. Активное вещество - тегасерод. Оно положительно влияет на моторную и эвакуаторную функцию толстого и тонкого кишечника. Способствует нормализации стула, уменьшает симптоматику раздраженного кишечника.
Не вызывает повышения давления, не оказывает влияния на сердечно-сосудистую систему. Однако существует достаточное количество побочных эффектов. В несколько раз повышается риск развития инсульта, стенокардии, развития ангинального приступа. В настоящее время препараты с этим активным веществом сняты с производства у нас и в ряде других стран для дальнейших исследований. Сюда относятся следующие прокинетики (список препаратов):
- «Тегасерод».
- «Зелмак».
- «Фрактал».
Антагонисты 5-НТЗ-рецепторов
Прокинетики этой группы подходят для лечения и профилактики тошноты и рвоты. При их приеме уменьшается время пребывания пищи в желудке, увеличивается скорость транзита пищи по кишечнику, нормализируется тонус толстого кишечника.

Наблюдается высвобождение ацетилхолина, и улучшается моторная функция ЖКТ. В настоящее время пользуются большим спросом у пациентов и врачей современные прокинетики. Список препаратов нового поколения:
- «Трописетрон».
- «Осетрон».
- «Ондасетрон».
- «Силансетрон».
Хочется отметить, что антагонисты 5-НТЗ-рецепторов не оказывают лечебного эффекта, если рвота вызвана апоморфином.
Эти препараты отлично переносятся, хотя имеются у них побочные эффекты:
- Головная боль.
- Запор.
- Приливы крови.
- Ощущения жара.
Еще один плюс этих препаратов - они не оказывают седативного действия, не взаимодействуют с другими лекарствами, не вызывают эндокринных изменений, не нарушают двигательную активность.
При каких заболеваниях назначают
Как говорилось выше, прокинетики используют в монотерапии или совместно с антибиотиками. Врачи знают, что имеются такие заболевания, при которых назначение прокинетиков в несколько раз повышает эффективность лечения. В эту группу можно отнести:
- Заболевания пищеварительной системы с нарушением моторной активности.
- Гастроэзофагельную рефлюксную болезнь.
- Язвенную болезнь желудка (двенадцатиперстной кишки).
- Идиопатический гастропарез.
- Рвоту.
- Запоры.
- Диабетический гастропарез.
- Метеоризм.
- Тошноту, вызванную лекарственной и радиотерапией, инфекцией, функциональными нарушениями, неправильным питанием.
- Диспепсию.
- Дискинезию желчевыводящих путей.

Кому нельзя принимать
Для препаратов группы прокинетики существуют противопоказания:
- Гиперчувствительность к активному веществу.
- Желудочные или кишечные кровотечения.
- или кишечника.
- Кишечная непроходимость.
- Острая печеночная недостаточность, нарушения работы почек.
Беременные и кормящие матери
Несколько слов хочется сказать о приеме препаратов при беременности. Исследования показали, что прокинетики имеют свойство проникать в грудное молоко, поэтому на период лечения такими лекарствами не следует продолжать кормление грудью.
В первый триместр беременности у женщин часто бывает рвота и тошнота. В этом случае возможно назначение таких лекарств, как прокинетики. Список препаратов для беременныхбудет включать в себя только те, которые не представляют угрозы для жизни беременной женщины и для плода.
Польза от него должна превышать все возможные риски. Прокинетики с активным веществом метоклопромид могут быть использованы из этой группы только по назначению врача. В последующие триместры беременности прокинетики не назначают.
В настоящее время препараты этой группы при беременности не назначают из-за большого количества побочных эффектов.
Прокинетики для детей
Применять прокинетики с активным веществом метоклопрамид у детей следует собенно осторожно, так как есть риск возникновения дискинетического синдрома. Его назначают в зависимости от веса ребенка.
Если педиатр назначает прокинетики, "Мотилиум" чаще всего входит в этот перечень. Он обладает хорошей переносимостью и имеет много положительных отзывов. Но могут быть назначены и другие прокинетики. Список препаратов для детей может содержать еще следующие названия:
- «Домперидон».
- «Метоклопромид».
Стоит отметить, что детям до 5 лет препарат "Мотилиум" рекомендуется использовать в виде суспензии. Лекарство назначают в зависимости от веса ребенка, из расчета 2,5 мл на каждые 10 кг веса. Если есть необходимость, дозу можно увеличивать, но только для малышей старше года. Также препарат выпускается в форме таблеток для рассасывания.

Прокинетики детям назначают, если у ребенка наблюдаются:
- Рвота.
- Тошнота.
- Эзофагит.
- Замедленное переваривание пищи.
- Диспептические симптомы.
- Частые срыгивания.
- Желудочно-пищеводный рефлюкс.
- Нарушение моторики желудочно-кишечного тракта.
Следует отметить, что в самые первые месяцы жизни организм ребенка и все его функции не очень развиты, поэтому все препараты следует принимать под строгим наблюдением и контролем врача. В случае передозировки прокинетики могут вызвать неврологические побочные эффекты у детей грудного и младшего возраста.
Большой популярностью у родителей грудничков пользуется растительный препарат, улучшающий пищеварение и уменьшающий газообразование в кишечнике. Это концентрат на основе плодов фенхеля «Плантекс».
Стоит сказать несколько слов о растительных прокинетиках.
Природные помощники
Так устроен мир, что лекарство от любого недуга можно найти в каком-нибудь растении, нужно знать только - в каком. Так, известны растительные прокинетики, которые стимулируют моторную функцию ЖКТ. Вот некоторые из них:
- Фенхель обыкновенный.
- Ромашка аптечная.
- Бузина черная.
- Укроп.
- Душица.
- Пустырник.
- Одуванчик.
- Мелисса.
- Сушеница болотная.
- Подорожник большой.
- Крушина ольховидная.
Список растений, помогающих улучшить моторику желудочно-кишечного тракта, включает в себя большое количество и других представителей флоры. Также следует учитывать, что некоторые овощи и фрукты оказывают аналогичный эффект:
- Брюква.
- Дыня.
- Капуста.
- Морковь.
- Свекла.
- Тыква.
- Брусника.
- Виноград.

Очень хорошо проявляются свойства прокинетиков у этих овощей, если принимать приготовленные из них свежие соки.
Стоит отметить, что не следует заменять лекарственные препараты растительными в периоды обострения заболеваний и без консультации с врачом.
Побочные эффекты
Очень важно, что прокинетики нового поколения имеют гораздо меньшее количество побочных эффектов, чем препараты первого поколения с активным веществом метоклопрамид. Однако и у самых новых лекарств отмечаются побочные явления:
- Головная боль.
- Повышенная возбудимость.
- Сухость во рту, жажда.
- Спазм гладкой мускулатуры органов желудочно-кишечного тракта.
- Крапивница, сыпь, зуд.
- Гиперпролактинемия.
- У малышей могут проявляться экстрапирамидные симптомы.
После отмены препарата побочные явления полностью проходят.
Если врач назначает прокинетики, список препаратов может включать несколько лекарств с разными названиями, но с одним активным действующим веществом. При этом побочные явления будут одинаковыми.
Особенности использования прокинетиков
Очень осторожно следует назначать прокинетики людям с печеночной недостаточностью и при плохой работе почек. Такие больные должны быть под строгим наблюдением врача.
При длительном использовании прокинетиков пациенты также должны чаще посещать лечащего врача. С осторожностью использовать прокинетики у детей младшего возраста, особенно до одного года.
Осторожно надо назначать препараты из этой группы пациентам пожилого возраста.
При лечении прокинетиками не стоит заниматься работой, требующей повышенного внимания и быстрой реакции.
Перед приемом следует обязательно проконсультироваться с доктором. От этого зависит ваше здоровье. Не стоит медицинский препарат заменять на его растительный аналог без предварительной консультации с врачом.
Допамин является нейротрансмиттером из группы катехоламинов, регулирующим различные функции центральной и периферической нервных систем, включая поведение, синтез и высвобождение гормонов и нейротрансмиттеров, а также кровяное давление и внутриклеточный транспорт ионов . Роль допаминергической иннервации в регуляции деятельности желудочно-кишечного тракта (ЖКТ) по сравнению с таковой в нервной системе изучена меньше. По-прежнему существуют противоречия во взглядах на источник допамина (нейрональный или ненейрональный) в ЖКТ . Тем не менее, антидопаминергические препараты, в частности домперидон, многие годы чрезвычайно эффективно используются для коррекции таких нарушений двигательной функции верхних отделов пищеварительной системы, как функциональная диспепсия (ФД), нарушение опорожнения желудка различного генеза, тошнота и рвота. Изучение влияния допамина на различные функции мозга привели к появлению гипотезы о существовании нескольких подтипов рецепторов допамина. Ранние исследования позволили выявить два класса рецепторов: D 1 и D 2 . Дальнейшая гетерогенность рецепторов была изучена с использованием метода клонирования, который показал существование по крайней мере пяти подтипов рецепторов допамина (D 1 -D 5) . Данный обзор посвящен роли дофаминергической системы в регуляции деятельности ЖКТ и сосредоточен на D 2 -подтипе рецепторов допамина. В частности, обсуждаются клинические проявления блокады D 2 -рецепторов таким эффективным прокинетическим препаратом, как домперидон, в том числе в ЖКТ (прокинетический терапевтический эффект) и центральной нервной системе (противорвотный эффект).
Многочисленные гистохимические и иммуногистохимические исследования строения стенки кишечной трубки млекопитающих продемонстрировали наличие нескольких популяций нейронов, содержащих амины, которые могут участвовать в регуляции моторики ЖКТ. Эти группы нейронов включают в том числе и норадренергические нейроны, имеющие происхождение из экстраорганной симпатической нервной системы. Они содержат допамин, который выступает как промежуточный продукт метаболизма в процессе формирования норадреналина . В то же время значительное количество допамина в организме не преобразуется в другие катехоламины, что предполагает существование периферической дофаминергической системы, независимой от симпатической норадренергической системы . Ткань тела желудка морских свинок спонтанно продуцирует допамин в количестве, сопоставимом с таковым в центральных дофаминергических нейронах. Высвобождение допамина увеличивается при трансмуральной электрической стимуляции через механизм, чувствительный к тетродотоксину (блокатор нейрональных Na + -каналов), и зависит от концентрации внеклеточного Ca 2+ , что предполагает нейрональный механизм высвобождения . И в организме человека, в тканях ЖКТ, селезенки и поджелудочной железы синтезируется значительное количество допамина . Сопоставление количества допамина и его метаболитов, синтезирующегося во внутренних органах с объемом, удаляемым почками, указывает на то, что до 46% допамина, сформированного в организме, не метаболизируется в норадреналин. Источник этого значительного количества допамина частично представлен не-нейрональными клетками дофаминергической паракринной системы в слизистой оболочке ЖКТ .
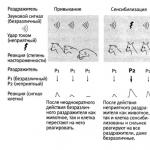
Как сам допамин, так и агонисты допаминовых рецепторов могут оказывать и тормозящее, и стимулирующее действие на двигательную функцию пищеварительного тракта (рис.). Тормозящее действие состоит в расслаблении мышечного слоя стенки и угнетении перистальтики пищеварительной трубки, которые наблюдаются от пищевода до толстой кишки . Известны убедительные работы, демонстрирующие способность допамина приводить к расслаблению стенки желудка в экспериментах на живых собаках . Гораздо реже по сравнению с тормозящим может наблюдаться и стимулирующее действие допамина .
К настоящему времени изучены гены, кодирующие пять подтипов допаминергических рецепторов. Эти пять рецепторов допамина принадлежат к надсемейству G-белок-связанных рецепторов и структурно характеризуются наличием семи трансмембранных доменов, которые связывают допамин. Из этих пяти подтипов D 1 - и D 5 -рецепторы объединены в подсемейство D 1 -подобных рецепторов, потому что имеют до 80% гомологичных аминокислотных последовательностей в трансмембранных доменах. Аналогично рецепторы D 2 , D 3 и D 4 , также демонстрирующие значительное подобие, классифицируются как члены подсемейства D 2 -подобных рецепторов. Эти два подсемейства отличаются тем, что активация D 1 -подобных рецепторов стимулирует выработку аденилатциклазы, тогда как активация D 2 -подобных рецепторов препятствует таковой . D 1 -рецепторы расположены в основном на постсинаптической мембране эффекторных клеток, тогда как D 2 -рецепторы расположены и пост-, и пресинаптически. В последнем случае они оказывают негативное модулирующее влияние на высвобождение ацетилхолина из внутренних холинергических нервных терминалей .
Убедительным доказательством того, что допамин играет существенную роль в регуляции моторики ЖКТ, служит тот факт, что антагонисты рецепторов допамина активно стимулируют двигательную функцию ЖКТ начиная от пищевода и заканчивая толстой кишкой. Домперидон, селективный антагонист D 2 -рецепторов, в частности, существенно улучшает антродуоденальную координацию . Также было установлено, что этот препарат блокирует тормозящий эффект допамина на моторику желудка и усиливает сократительную активность толстой кишки у здоровых добровольцев .
На животных моделях стимуляция D 2 -допаминовых рецепторов (с помощью апоморфина или непосредственно допамина) на уровне триггерной зоны широко используется для изучения рвоты и связанных с ней изменений двигательной активности ЖКТ . Рвота (то есть насильственное изгнание желудочно-кишечного содержимого через рот) является высокоорганизованным процессом, координируемым центром рвоты, который получает импульсы от нескольких периферических и центральных рецепторных полей. Этот процесс включает в себя следующие события. Расслабление желудка начинается за несколько минут до появления гигантского ретроградного сокращения (ГРС) тонкой кишки и достигает максимума к моменту достижения ГРС антрума. ГРС появляется в средней части тонкой кишки и движется по направлению к антруму со скоростью 5-10 см/сек. Его появлению предшествует торможение перистальтики тонкой кишки и исчезновение медленных волн . После прохождения ГРС следуют фазы повышения и снижения тонуса кишки. Данные изменения моторики всегда сопровождают рвоту, но могут наблюдаться и независимо от нее . Блокада ретроградной двигательной активности, которая сопровождает тошноту и рвоту, может вносить вклад в общее прокинетическое действие антидопаминергических препаратов.
Предположение о том, что блокада допаминовых рецепторов может привести к прокинетическому действию, имеет обоснование в тех наблюдениях, которые свидетельствуют об очень широком распространении допамина в стенке пищеварительной трубки, где он оказывает отчетливое действие на моторику: уменьшает тонус нижнего пищеводного сфинктера, снижает тонус стенки желудка, уменьшает внутрижелудочное давление и угнетает гастродуоденальную координацию . Поэтому блокада данных ингибирующих D 2 -допаминовых рецепторов селективными антагонистами оказывает прокинетический эффект. Кроме того, у домперидона можно предположить и наличие еще одного механизма, объясняющего его прокинетическое воздействие. Ряд работ продемонстрировал ингибирующий эффект допамина на стимулированное сокращение гладкомышечных клеток желудка морских свинок, обусловленный активацией альфа-2-адренорецепторов . Впоследствии было установлено, что допамин угнетает высвобождение ацетилхолина в желудке морских свинок путем активации пресинаптических D 2 -рецепторов, и данный эффект снижается при применении домперидона, который, в свою очередь, отчетливо стимулирует сокращения стенки желудка . Таким образом, по меньшей мере, на животных моделях, было показано наличие холинергического механизма прокинетического действия домперидона.
Домперидон как антидопаминергический препарат, обладающий прокинетическим действием, в клинической практике нашел применение в лечении диспепсических расстройств и тошноты и показан при лечении пациентов с ФД, гастропарезом различного генеза, включая диабетический, а также для предупреждения и купирования тошноты и рвоты.
Были проведены многочисленные клинические исследования, продемонстрировавшие эффективность домперидона при лечении этих состояний . Подробный анализ этих исследований лежит за рамками данной работы, но, тем не менее, среди них следует упомянуть работу Sturm, доказавшую большую эффективность домперидона по сравнению с метоклопрамидом в лечении гастропареза , а также метаанализ, который провели V. Van Zanten et al., продемонстрировавший эффективность домперидона в лечении ФД и установивший его семикратное превосходство над плацебо — отношение шансов (ОШ) 7,0 (95% ДИ, 3,6-16) . Это несомненно делает Мотилиум® (оригинальный домперидон) препаратом выбора в лечении больных с ФД.
Мотилиум® (оригинальный домперидон) плохо проникает через гематоэнцефалический барьер, что, с одной стороны, подчеркивает его безопасность, с другой стороны, делает препаратом выбора для предупреждения и устранения тошноты, в том числе индуцированной применением L-DOPA у больных с болезнью Паркинсона , при проведении химиотерапии, после хирургических вмешательств, при мигрени. Экстрапирамидные расстройства при применении домперидона встречаются редко, в отличие от других препаратов данной группы, в частности метоклопрамида .
Таким образом, изучение механизмов влияния допамина на двигательную функцию пищеварительного тракта, особенностей функционирования рецепторов допамина позволили внедрить в практику один из самых эффективных классов гастроэнтерологических препаратов — селективные антагонисты D 2 -рецепторов. Наиболее изученным в многочисленных исследованиях, доказавшим свою эффективность в клинической практике представителем этого класса является Мотилиум® (оригинальный домперидон).
Литература
- Palermo-Neto J. Dopaminergic systems. Dopamine receptors // Psychiatr Clin North Am. 1997; 20: 705-721.
- Willems J. L., Buylaert W. A., Lefebvre R. A., Bogaert M. G. Neuronal dopamine receptors on autonomic ganglia and sympathetic nerves and dopamine receptors in the gastrointestinal system // Pharmacol Rev. 1985; 37: 165-216.
- Mann R., Bell C. Distribution and origin of aminergic neurones in dog small intestine // J Auton Nerv Syst. 1993; 43: 107-115.
- Eisenhofer G., Aneman A., Friberg P. et al. Substantial production of dopamine in the human gastrointestinal tract // J Clin Endocrinol Metab.1997; 82: 3864-3871.
- Hartman D. S., Civelli O. Dopamine receptor diversity: molecular and pharmacological perspectives // Prog Drug Res. 1997; 48: 173-194.
- Sidhu A. Coupling of D1 and D5 dopamine receptors to multiple G proteins: implications for understanding the diversity in receptor-G protein coupling // Mol Neurobiol. 1998; 16: 125-134.
- Kopin I. J. Catecholamine metabolism: basic aspects and clinical significance // Pharmacol Rev. 1985; 37: 333-364.
- Shichijo K., Sakurai-Yamashita Y., Sekine I., Taniyama K. Neuronal release of endogenous dopamine from corpus of guinea pig stomach // Am J Physiol.1997; 273: G1044-1050.
- Valenzuela J. E. Dopamine as a possible neurotransmitter in gastric relaxation // Gastroenterology. 1976; 71: 1019-1022.
- Crocker A. D. A new view of the role of dopamine receptors in the regulation of muscle tone // Clin Exp Pharmacol Physiol. 1995; 22: 846-850.
- Tonini M. Recent advances in the pharmacology of gastrointestinal prokinetics // Pharmacol Res. 1996; 33: 217-226.
- Schuurkes J. A., Van Nueten J. M. Domperidone improves myogenically transmitted antroduodenal coordination by blocking dopaminergic receptor sites // Scand J Gastroenterol Suppl. 1984; 96: 101-110.
- Nagahata Y., Urakawa T., Kuroda H. et al. The effect of dopamine on rat gastric motility // Gastroenterol Jpn. 1992; 27: 482-487.
- Wiley J., Owyang C. Dopaminergic modulation of rectosigmoid motility: action of domperidone // J Pharmacol Exp Ther. 1987; 242: 548-551.
- Wang S. C., Borison H. L. A new concept of organization of the central emetic mechanism: recent studies on the sites of action of apomorphine, copper sulfate and cardiac glycosides // Gastroenterology. 1952; 22: 1-12.
- Lang I. M., Sarna S. K., Condon R. E. Gastrointestinal motor correlates of vomiting in the dog: quantification and characterization as an independent phenomenon // Gastroenterology. 1986; 90: 40-47.
- De Ponti F., Malagelada J. R., Azpiroz F., Yaksh T. L., Thomforde G. Variations in gastric tone associated with duodenal motor events after activation of central emetic mechanisms in the dog // J Gastrointest Motil. 1990; 2: 1-11.
- De Ponti F. Pharmacology of emesis and gastrointestinal motility: implications for migraine // Funct Neurol. 2000; 15 (Suppl. 3): 43-49.
- Demol P., Ruoff H. J., Weihrauch T. R. Rational pharmacotherapy of gastrointestinal motility disorders // Eur J Pediatr. 1989; 148: 489-495.
- Costall B., Naylor R. J., Tan C. C. The mechanism of action of dopamine to inhibit field stimulation-induced contractions of guinea pig stomach strips // Naunyn Schmiedebergs Arch Pharmacol. 1984; 328: 174-179.
- Kusunoki M., Taniyama K., Tanaka C. Dopamine regulation of acetylcholine release from guinea-pig stomach // J Pharmacol Exp Ther. 1985; 234: 713-719.
- Soykan I., Sarosiek I., McCallum R. W. The effect of chronic oral domperidone therapy on gastrointestinal symptoms, gastric emptying, and quality of life in patients with gastroparesis // Am J Gastroenterol. 1997; 92: 976-980.
- Barone J. A. Domperidone: a peripherally acting dopamine2-receptor antagonist // Ann Pharmacother. 1999; 33: 429-440.
- Sturm A., Holtmann G., Goebell H., Gerken G. Prokinetics in patients with gastroparesis: a systematic analysis // Digestion. 1999; 60: 422-427.
- Veldhuyzen van Zanten S. J., Jones M. J., Verlinden M., Talley N. J. Efficacy of cisapride and domperidone in functional (nonulcer) dyspepsia: a meta-analysis // Am J Gastroenterol. 2001; 96: 689-696.
- Soykan I., Sarosiek I., Shifflett J., Wooten G. F., McCallum R. W. Effect of chronic oral domperidone therapy on gastrointestinal symptoms and gastric emptying in patients with Parkinson’s disease // Mov Disord. 1997; 12: 952-957.
- Pinder R. M., Brogden R. N., Sawyer P. R., Speight T. M., Avery G. S. Metoclopramide: a review of its pharmacological properties and clinical use // Drugs. 1976; 12: 81-131.
- Brogden R. N., Carmine A. A., Heel R. C., Speight T. M., Avery G. S. Domperidone. A review of its pharmacological activity, pharmacokinetics and therapeutic efficacy in the symptomatic treatment of chronic dyspepsia and as an antiemetic // Drugs. 1982; 24: 360-400.
- Sol P., Pelet B., Guignard J. P. Extrapyramidal reactions due to domperidone // Lancet. 1980; 2: 802.
А. С. Трухманов, доктор медицинских наук, профессор
Точный контроль и настройка передачи нервных импульсов в центральную нервную систему ответственны за нормальный ход ряда важных процессов.
Так, например, активность дофаминовых рецепторов в определенных структурах мозга отвечает за контроль над движением, настроение, эмоциональный статус. Нарушения (изменения активности рецептора, увеличение или уменьшение уровней дофамина в головном мозге) приводят к развитию различных заболеваний.
Дофамин по существу является одним из основных нейротрансмиттеров (веществ в мозге, ответственных за передачу информации) и относится к группе катехоламинов.
Различные исследования в области показывают, что с возрастом и под влиянием определенных эндогенных факторов (генетическая предрасположенность, высокий уровень свободных радикалов и т. д.) и экзогенных факторов (уровень загрязнения окружающей среды, лекарств, травм, болезней) уровень дофамина в мозге значительно уменьшается. Со временем и при наличии резких потерь дофамина медленно, постепенно, серьезные травмы развиваются с серьезными последствиями в долгосрочной перспективе.
Чтобы влиять и контролировать этот процесс, современная медицина активно развивает и внедряет в клиническую практику препараты, которые демонстрируют высокую активность и эффективность (достижение желаемых результатов у большого процента пациентов) на фоне хорошего профиля безопасности (низкий риск развития серьезных побочных эффектов). Именно этот тип препарата называется агонистом дофамина.
Что такое агонисты дофамина?
Агонисты дофамина, как следует из их названия, активируют специфические рецепторы допамина в центральной нервной системе (головном мозге) и приводят к идентичности с природными, эндогенными дофаминовыми эффектами. Термин «агонист» указывает, что эти препараты имеют выраженное сродство к дофаминовым рецепторам (способность связываться с ними), а также активность (способность связывать рецепторы, вызывающие связанные эффекты).
Агонисты дофамина представляют собой группу препаратов, которые подвергаются развитию, улучшают свои свойства и разрабатывают новые эффективные агенты с лучшей абсорбцией, активностью и долгосрочными эффектами и улучшают профиль безопасности.
Развитие современной медицины и фармацевтической промышленности позволяет синтезировать препараты с точным механизмом действия и реагированием на специфические рецепторы в структурах головного мозга, соответственно тонким контролем и контролем желаемых эффектов.
Для агонистов дофамина целевыми рецепторами являются рецепторы дофамина (D1, D2, D3 и D4), наиболее важным для клинической практики является ответ типа D2-дофаминового рецептора.
Их активация приводит к аналогичному эффекту в результате синтеза в основном дофамин тела, влияющие двигательные действия (точное управление движением, двигательная активность), память и познавательные потенциального в целом, но и эмоциональное равновесие (стабильность настроения), репродуктивное здоровья (путем контроля уровней пролактина).
При дефиците дофамина, например, болезнь Паркинсона развивается, а на слишком высоких уровнях можно развить различные психические и поведенческие расстройства, включая шизофрению.
Когда принмиать агонисты дофамина?
В болезни Паркинсона выявлены дегенеративные изменения дофаминергических нейронов основной нигры. Характерным является дефицит дофамина и нарушенное соотношение дофамина и ацетилхолина. Прямое введение дофамина в организм не влияет, поскольку не проходит через гематоэнцефалический барьер. Поэтому вводят предшественник дофамина, такой как L-DOPA. Очень скоро после начала терапии возникают побочные эффекты, такие как гиперкинезия, аритмии, ортостат, агрессивность и т. д., Что требует включения агонистов дофамина в терапию. Они активируют дофаминовые рецепторы в отсутствие дофамина
Различные представители этой фармакологической группы преимущественно используются в дефиците (слишком низких уровнях) дофамина в мозге, что наблюдается, например, при болезни Паркинсона.
Болезнь Паркинсона по существу является нейродегенеративным заболеванием из-за снижения уровней дофамина и дисбаланса некоторых других нейротрансмиттеров с характерными симптомами. Чаще всего из-за низкого уровня дофамина наблюдается повреждение тонкой двигательной активности (тремор, несогласованные движения, мышечная ригидность), но и различные психоневрологические события (проблемы со сном, что приводит к частой бессоннице, снижение когнитивной способности, ухудшение памяти и другие).
Не совсем понятны причины развития этого заболевания, но обсуждался ряд факторов (генетическая предрасположенность, возраст, мужской пол, неблагоприятные последствия воздействия окружающей среды пестицидов и тяжелые металлы и т.д.). Основой заболевания является дефицит дофамина.
Другие заболевания, которые развиваются при нарушениях метаболизма дофамина и балансе связаны с реакцией пролактина гомеостаза и включают в себя различные нарушения репродуктивной функцию, аменорею, импотенцию, акромегалии, эректильную дисфункцию, гиперпролактинемию и связанные с ним осложнения, а также для ингибирования лактации.
Препараты этой группы также применяются к некоторым неврологическим заболеваниям, связанным с недостаточностью допамина, некоторыми неопластическими формами и др.
Как правило, препараты используются для первичной и разовой терапии (только агонист дофамина) или как часть комплексной терапии (в сочетании с другими препаратами и лечебными процедурами) при следующих условиях:
- Болезнь Паркинсона
- Лекарственная дистония
- Синдром беспокойных ног
- Рассеянный склероз
- Доброкачественное новообразование гипофиза
- Первичная аменорея
- Вторичная аменорея
- Аменорея неуточненная
- Гиперпролактинемия
- Поликистозный овариальный синдром
- Импотенция органического происхождения
- Сексуальная дисфункция, не вызванная органическим расстройством или заболеванием, в частности при отсутствии генитальной реакции
- Акромегалия и гипофизарный гигантизм
Наиболее широко используются методы лечения болезни Паркинсона, которые используются в качестве альтернативы стандартной терапии леводопой или как средство снижения потребности в высоких дозах леводопы. Использование этих препаратов на ранних стадиях заболевания приводит к значительной задержке в необходимости леводопы, эффективно влияя на моторные нарушения.
У пациентов с прогрессирующим заболеванием сопутствующее применение агонистов допамина и леводопы и производных приводит к уменьшению требуемой терапевтической дозы.
В целом рекомендуется использовать пациентов с активным возрастом с недавно обнаруженной болезнью и мягкими проявлениями, при этом режим лечения учитывает индивидуальные характеристики пациента. Чаще всего начинается лечение агонистами дофамина и низкими дозами леводопы или монотерапией с соответствующими агонистами дофамина.
Агонисты допамина: агенты и путь введения
Индивидуальные агенты доступны в разных лекарственных формах для достижения оптимального эффекта у отдельных пациентов.
Их чаще всего вводят перорально (в виде таблеток, капсул, препаратов с пролонгированным высвобождением), некоторые из них доступны для парентерального введения (внутривенная инфузия, подкожная инъекция), а также для так называемых трансдермальных терапевтических систем (участки кожи, которые обеспечивают равномерное и контролируемое высвобождение активного вещества).
Есть несколько основных представителей этой группы:
- бромокриптин: широко используется в различных нарушениях дефицита дофамина, таких как гиперпролактинемия, нарушения менструального цикла, ингибирование лактации (ингибирование), болезнь Паркинсона и тому подобное. При использовании в сочетании с леводопой у пациентов с болезнью Паркинсона, это позволяет снизить дозу леводопы на 30% (что значительно снижает риск серьезных побочных эффектов, связанных с этим лекарственным средством)
- перголид: используется главным образом в различных режимах лечения болезни Паркинсона
- Каберголин: он имеет длительный период полувыведения плазмы, и различные исследования, проведенные с ним, демонстрируют высокую эффективность и использование в виде монотерапии в течение по меньшей мере одного года на ранних стадиях болезни Паркинсона
- ропинирол: особенно популярный препарат для лечения ранних стадий болезни Паркинсона, демонстрирующий высокую эффективность и отсрочку леводопы
- прамипексол: лекарственный продукт, который эффективно влияет на двигательные симптомы у пациентов с нейродегенеративными заболеваниями и, в частности, с болезнью Паркинсона
- Апоморфин: он был впервые использован более 60 лет назад, но быстро потерял популярность из-за неприятных побочных эффектов, связанных с его использованием (сильная тошнота и рвота, но после улучшения его формулы в 1990 году она снова является препаратом выбора, особенно в тяжелых формы болезни Паркинсона
Доза и режим лечения индивидуально определяются для каждого пациента после тщательного обследования и обследования специалистом.
Самостоятельные корректировки лечения создают значительные риски для их общего состояния.
Возможные побочные эффекты (нежелательные эффекты) с терапией агонистом дофамина
Агонисты допамина, как и все известные лекарства, имеют определенные риски возникновения нежелательных эффектов. В зависимости от степени тяжести незначительные, умеренные и серьезные побочные эффекты различаются, и трудно предсказать реакцию организма на отдельных пациентов.
Индивидуальные характеристики пациента, наличие основных заболеваний, потребление других лекарств, повышенная чувствительность к любому из ингредиентов, возраст и т. д. Также важны для определения риска возникновения нежелательных эффектов.
Некоторые побочные эффекты, наблюдаемые при терапии агонистом дофамина, включают следующее:
- тошнота и рвота
- дискомфорт в желудке
- зрительные и слуховые галлюцинации
- головная боль
- путаница, головокружение
- отмеченная сонливость в течение дня
- сухость во рту
- ортостатическая гипотония
- поведенческие изменения (компульсивное переедание, гиперсексуальность и т. д.)
Некоторые побочные эффекты предсказуемы и распространены (например, тошнота и рвота), могут быть приняты профилактические меры, такие как использование соответствующих противорвотных средств.
Хотя редко может ухудшать функцию почек, расстройства печени, анемию, фиброз легких и другие.
Чтобы снизить риск побочных эффектов и взаимодействий, сообщите врачу обо всех лекарствах, которые вы принимаете (с рецептом или без рецепта, включая пищевые добавки).
Особая осторожность когда препараты группы агонистов дофамина вводятся с одновременным применением антигипертензивных агентов (для лечения высокого кровяного давления), определенных антибиотиков, антидепрессантов, диуретиков и др.
2. Антагонисты гистаминовых h1рецепторов
a. антагонисты гистаминовых H 1 рецепторов включаютдифенгидрамин [Димедрол, Benadryl],парахлорамин ,циклизин ,dimenhydrinate иpromethazine .
b. наиболее вероятным действием этих средств является ингибирование холинергических проводящих путей от вестибулярного аппарата.
c. антагонисты гистаминовых H 1 рецепторов используются приморской болезни, истинном головокружении и тошноте беременности .
d. эти средства вызывают седативный эффект и ксеростомию.
3. Антагонисты допамина
a. Метоклопрамид
(1) Метоклопрамид блокирует рецепторы в пределах CTZ.
(2) Метоклопрамид увеличивает чувствительность желудочно-кишечного тракта к действие ацетилхолина (ACh); это усиливает желудочно-кишечную перистальтику,желудочную эвакуацию и увеличивает тонус нижнего пищеводного сфинктера.
(3) Большие дозы метоклопрамида проявляют антагонизм в отношении серотониновых (5-HT 3) - рецепторов в рвотном центре и желудочно-кишечном тракте.
(4) Метоклопрамид используется для уменьшениятошноты, вызванной химиотерапией , при использовании таких средств какцисплатин и доксорубицин и вызванной наркотиками рвотой.
(5) Метоклопрамид обладает седативным эффектом, вызывает понос, эктрапирамидальные расстройства и повышает секрецию пролактина.
b. Фенотазины и производные бутирофенона
(1) производные фенотиазина: алифатические -хлорпромазин* (аминазин) ; пиперидиновые -тиоридазин ; пиперазиновые -флуфеназин, трифлуоперазин (трифтазин) ; производные бутирофенона –галоперидол*, дроперидол ;.
(2) Фентиазины и бутирофеноны блокируют допаминергические рецепторы в CTZ и замедляют периферическую передачу к рвотному центру.
(3) Эти средства используются притошноте вследствие химиотерапии и лучевой терапии, и для управления послеоперационной тошнотой .
(4) Неблагоприятные эффекты (неярко выраженные для производных бутирофенона) включают: антихолинергические последствия (сонливость, ксеростомия и потеря остроты зрения), экстрапирамидальные расстройства и ортостатическая гипотония. Противопоказанием к назначению этих средств является болезнь Паркинсона.
c. В последние годы среди антагонистов дофаминовых рецепторов, регулирующих моторную функцию желудочно-кишечного тракта и оказывающих противорвотное действие, внимание исследователей и практических врачей все больше привлекаетдомперидон [Мотилиум] . Это антагонист периферических и центральных дофаминовых рецепторов, обладающий аналогичнометоклопрамиду и некоторымнейролептикам противорвотными и противотошнотными свойствами, однаконе обладающий хорошей проницаемостью через гематоэнцефалитический барьер . К тому же метоклопрамид, даже назначаемый по 10 мг 4 раза в сутки, не всегда эффективен при хроническом парезе желудка; кроме того, он часто оказывает побочное действие в виде дискинезии и сонливости. Противорвотное действиедомперидона обусловлено сочетанием гастрокинетического (периферического) действия и антогонизма к рецепторам дофамина в триггерной зоне хеморецепторов головного мозга, т.е. осуществлениемблокады периферических и центральных дофаминовых рецепторов .Домперидон оказался эффективным в устранении тошноты и рвоты различного происхождения, очевидно, и благодаря увеличению продолжительности перистальтических сокращений антрального отдела желудка и двенадцатиперстной кишки, ускорению опорожнения желудка и повышению тонуса нижнего сфинктера пищевода.Показания к применению домперидона: диспептический синдром, тошнота и рвота различного происхождения - функционального, органического, инфекционного, диетического, а также ассоциированного с радиотерапией или лекарственной терапией, особенно с антипаркинсоническими средствами - антагонистами дофамина, например леводопой, бромокриптином (в качестве специфического средства). При острых и подострых состояниях (при тошноте и рвоте) домперидон обычно назначают взрослым и детям старше 12 лет по 20 мг 3-4 раза в сутки за 15-30 мин до еды и перед сном; детям от 5 до 12 лет - по 10 мг 3-4 раза в сутки за 15-30 мин до еды и вечером, перед сном. В остальных случаях (при хронической диспепсии) домперидон назначают взрослым по 10 мг 3 раза в сутки за 15-30 мин до еды, в случае необходимости и перед сном; детям в возрасте от 5 до 12 лет - по 10 мг 3 раза в сутки также за 15-30 мин до еды, в случае необходимости и вечером, перед сном.
d. Диметпрамид
(1) Блокирует дофаминовые D 2 -рецепторы триггерной зоны рвотного центра, стимулирует кровоснабжение и моторику органов ЖКТ. При в/м введении эффект проявляется через 30-40 мин, при приеме внутрь - через 50-60 мин, сохраняется в течение 4-5 ч. Не кумулирует.
(2) Показания: Предупреждение и купирование тошноты и рвоты, в т.ч. в послеоперационном периоде, при лучевой и химиотерапии онкологических больных, при заболеваниях ЖКТ.
(3)Противопоказания: Гиперчувствительность.
Нарушение функции почек и печени, выраженная гипотензия.
(5) Побочные действия: Аллергические реакции; умеренное понижение АД и сонливость (при использовании больших доз).
(6) Способ применения и дозы: Внутрь (до еды) или в/м: по 0,02 г 2-3 раза в сутки. Максимальные дозы (внутрь и в/м) - 0,1 г/сут. Курс - 2-4 нед в зависимости от характера заболевания, эффективности и переносимости диметпрамида. При нарушении функции почек и печени, выраженной гипотензии суточная доза не должна превышать 0,04 г.
(7) Меры предосторожности: У пациентов с нарушением функции почек и печени, выраженной гипотензией необходим регулярный (каждые 2-3 дня) контроль АД и функциональное исследование паренхиматозных органов.
e. Тиэтилперазин
(1) Угнетает рвотный центр, блокирует триггерную зону в продолговатом мозге. Оказывает адренолитическое и м-холиноблокирующее действие. Связывает дофаминовые рецепторы в нигростриарных путях, но, в отличие от нейролептиков, не имеет антипсихотических, антигистаминных и каталептогенных свойств. После приема внутрь быстро и полностью всасывается в ЖКТ. Подвергается биотрансформации в печени. Экскретируется почками.
(2) Показания: Тошнота и рвота (при лучевой и химиотерапии злокачественных новообразований, послеоперационный период).
(3) Противопоказания: Гиперчувствительность, нарушение функций печени и почек, закрытоугольная глаукома, гипотония, угнетение ЦНС, коматозное состояние, заболевания сердца и крови, аденома предстательной железы, болезнь Паркинсона и паркинсонизм, беременность.
(4) Ограничения к применению: Кормление грудью (на время лечения прекращают грудное вскармливание), детский возраст (до 15 лет).
(5) Побочные действия: Головная боль, головокружение, судороги, экстрапирамидные расстройства, ксеростомия, тахикардия, ортостатическая гипотония, фотосенсибилизация, пигментация сетчатки, периферические отеки, нарушения функций печени и почек, холестатический гепатит, агранулоцитоз, аллергические реакции.
(6) Взаимодействие: Усиливает эффект транквилизаторов, анальгетиков, бета-адреноблокаторов, гипотензивных средств, м-холиноблокаторов, алкоголя, снижает - адреналина, леводопы, бромокриптина.
(7) Способ применения и дозы: Для взрослых - по 10 мг внутрь, в/м или ректально 3 раза в сутки. Курс лечения - 2-4 нед.
| " |